Pada postingan kali ini aku ingin membahas mengenai bagaimana struktur dari suatu senyawa direpresentasikan. Struktur dari suatu senyawa dapat direpresentasikan dalam 4 tipe, yaitu struktur Lewis, struktur Kekule, struktur terkondensasi, dan struktur kerangka.
Pada struktur Lewis, kita bisa melihat ikatan, elektron pasangan bebas, dan muatan formal. Ikatan tersbuet tidak menggambarkan sudut dari ikatan dalam molekul nyatanya. Elektron pasangan bebas adalah elektron valensi yang tidak digunakan dalam ikatan dan juga biasanya disebut sebagai ikatan non-pengikatan. Sementara muatan formal adalah muatan yang dikandung oleh suatu atom. Kita dapat mengetahui berapa banyak muatan menggunakan formula berikut:
Pertama, berdasarkan pada formula di atas, coba hitung berapa muatan formal (formal charge) pada masing-masing atom.
Apabila muatan formal diberikan pada suatu atom, masing-masing atom menjadi memiliki nama spesifisik, seperti sebagai berikut:
Selanjutnya mari berlajar bagaimana menggambar struktur Lewis dari suatu molekul. Mari kita coba menggambar struktur HNO2.
Pesrtama, kita tentukan elektron valensi total dari HNO2, yaitu 1+5+12 = 18 elektron valensi, karena elektron valensi H = 1, elektron valensi N = 5, dan elektron valensi O = 6 (berhubung O nya ada 2, jadi 2x6 = 12).
Kedua, mari menggambar ikatan yang mungkin.
Kita bisa melihat terdapat 3 ikatana tunggal yang secara keseluruhan memiliki 6 elektron. Terakhir, kita bisa menggambar elektron pasangan bebas dengan mengurangi dari elektron valensi total dengan elektron total pada ikatan, 18-6 = 12. Artinya terdapat 12 elektron pasangan bebas. Kita harus memastikan meletakkan elektron pasangan bebas pada atom yang mungkin dan menghitung mautan formalnya yang harus sama dengan nol. Jika tidak nol, maka dapat mempertimbangkan adanya ikatan rangkap dua atau susun ulang strukturnya.
Pada atom H, tidak terdapat elektron pasangan bebas, karena semua elektron pada H (yaitu 1) habis terpakai untuk ikatan. Pada atom O pertama dari kiri, 2 elektron digunakan untuk ikatan, sehingga tersisa 4 elektron (6-2 = 4 elektron) yang tidak berikatan, artinya terdapat 2 elektron pasangan bebas. Selanjutnya pada atom N, 2 elektron digunakan untuk ikatan, sehingga tersisa 3 elektron (5-2 = 3 elektron), maka 1 pasangan bebas tersisa, dan 1 atom tidak berpasangan. Sementara O yang terakhir, 1 elektron digunakan untuk ikatan sehingga tersisa 5 elektron (6-1 = 5 elektron), artinya terbentuk 4 pasangan elektron bebas dan 1 atom tidak berpasangan.
Masing-masing dari 1 elektron pada N dan O yang tidak berpasangan dapat membentuk ikatan, sehingga di antara kedua atom tersebut terbentuk ikatan rangkap 2.
Apabila digambar seperti pada gambar di bawah ini, menjadi salah karena muatan formal tidak sama dengan nol. Mari kita hitung, muatan formal N pada gambar adalah 5 - (2+2) = 1, sementar O pada atom dengan warna merah 6 - (6+ 1) = -1. Sementara, seharusnya tidak ada muatan formal baik pada atom N dan O. Sehingga struktur ini menjadi salah.
Berbeda dengan struktur yang dengan ikatan rangkap 2, adalah struktur yang benar karena muatan formalnya = 0. Mari kita hitung, muatan formal atom N = 5 - (2+3) = 0, sementara untuk atom O = 6 - (4+2) = 0.
Kembali membahas struktur senyawa, setelah membahas struktur Lewis, struktur yang kedua adalah struktur Kekule. Meski digambar dengan cara yang sama dengan struktur Lewis, bedanya pada Kekule, elektron pasangan bebas tidak digambarkan. Mudah yaaa.
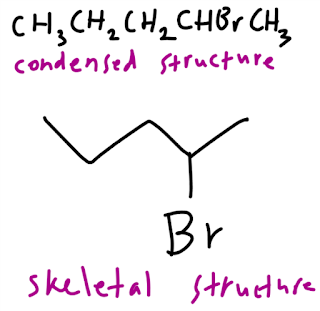
Sementara struktrur terkondensasi (condensed structure), senyawa tidak digambarkan dengan garis, sehingga hanya menyebutkan unsur-unsurnya saja dan garis dapat digambarkan hanya untuk menekankan adanya suatu gugus fungsi, misalnya:
Terakhir adalah struktur rangka (skeletal structure), dimana struktur ini berfokus hanya pada gugus fungsi yang penting saja, sementara atom karbon dengan hidrogennya pada ikatan, tidak ditunjukkan. Struktur rangka ini digambar sebagai berikut:
Berbicara mengenai struktur senyawa, di labku, struktur rangka yang lebih sering digunakan, karena memudahkan penggambaran dan hemat waktu.
Sekian mengenai struktur senyawa, semoga bisa dipahami dan dapat bermanfaat. Mohon maaf kalau ada salah. Terima kasih sudah berkunjung!





















0 comments:
Post a Comment
If you want to be notified that I've answered your comment, please leave your email address. Your comment will be moderated, it will appear after being approved. Thanks.
(Jika Anda ingin diberitahu bahwa saya telah menjawab komentar Anda, tolong berikan alamat email Anda. Komentar anda akan dimoderasi, akan muncul setelah disetujui. Terima kasih.)